
Eines der ältesten Unternehmen im Bereich Diabetes-Technologie ist Medtronic Diabetes, dessen Produktentwicklung sich im Laufe der Jahre weiterentwickelt hat.
Das Unternehmen ist seit Jahrzehnten führend bei Insulinpumpen und brachte als erstes Unternehmen ein kombiniertes Gerät mit einem kontinuierlichen Glukosemonitor (CGM) auf den Markt. Da es sich um einen mächtigen Marktführer in der Pharmaindustrie handelt, neigen Patienten dazu, eine Hassliebe zu diesem Unternehmen zu pflegen – ihre Angebote schätzen sie jedoch nicht immer ihren Kundenservice oder ihre Marketingtaktiken.
Wie auch immer man es betrachtet, Medtronic Diabetes ist führend in der Diabetes-Technologie, daher ist es wichtig zu wissen, was das Unternehmen tut. Hier finden Sie einen detaillierten Einblick in die Angebote von Medtronic Diabetes im Jahr 2020 und darüber hinaus:
Inhalt
Aktuelle Diabetes-Tools
Ab Mitte 2020 bietet Medtronic Diabetes folgende Technologietools an:
Minimierte 670G (hybrider geschlossener Regelkreis)
Der Minimed 670G war eine Premiere für unsere Diabetes-Community, da dieser erste Hybrid-Closed-Loop (HCL) im September 2016 die Zulassung der Food and Drug Administration (FDA) erhielt.

„Hybrid Closed Loop“ bedeutet einfach, dass das Insulinabgabesystem teilweise automatisiert ist, aber dennoch eine gewisse Kontrolle durch den Benutzer erfordert. Das offizielle FDA-Definition wird etwas technischer.
Die Funktionsweise besteht darin, dass der CGM-Sensor alle 5 Minuten Glukosedaten liest und der in die Pumpe integrierte „Closed-Loop“-Algorithmus diese Informationen verwendet, um die basale (Hintergrund-)Insulinabgabe zu erhöhen oder zu verringern, um den Glukosespiegel möglichst nahe beieinander zu halten bis zu einem festen Ziel von 120 mg/dL möglich (zum Entsetzen vieler Benutzer kann dieser Wert nicht angepasst werden).
Benutzer müssen immer Kohlenhydratmengen und Bolusmengen eingeben, um die Mahlzeiten abzudecken, und das System vor jeder Übung alarmieren. Es bietet auch keine automatischen CGM-basierten Korrekturboli, schlägt jedoch Korrekturmengen vor, wenn ein Blutzuckermesswert aus der Fingerbeere eingegeben wird.
Der 670G wurde 2017 mit großen Erwartungen auf den Markt gebracht, aber da es sich um eine frühe und noch begrenzte „künstliche Bauchspeicheldrüse“ mit offensichtlichen Einschränkungen handelte, stieß sie bei Menschen mit Diabetes nicht auf so positive Reaktionen, wie das Unternehmen gehofft hatte.
Weitere Informationen finden Sie in unserer 670G-Berichterstattung und in unseren Produktbewertungen.
Intelligenter Insulin-Pen: Companion InPen
Im August 2020 gab Medtronic Diabetes die Übernahme des Startups Companion Medical und des Bluetooth-fähigen Insulin-Pens, bekannt als InPen, bekannt. Es ist der einzige von der FDA zugelassene wiederverwendbare Insulinstift, der eine Verbindung zu einer App herstellt, um Daten zu verfolgen und Benutzern personalisierte Dosierungsempfehlungen für kurzwirksames Insulin (Humalog, Novolog, Fiasp) zu geben.

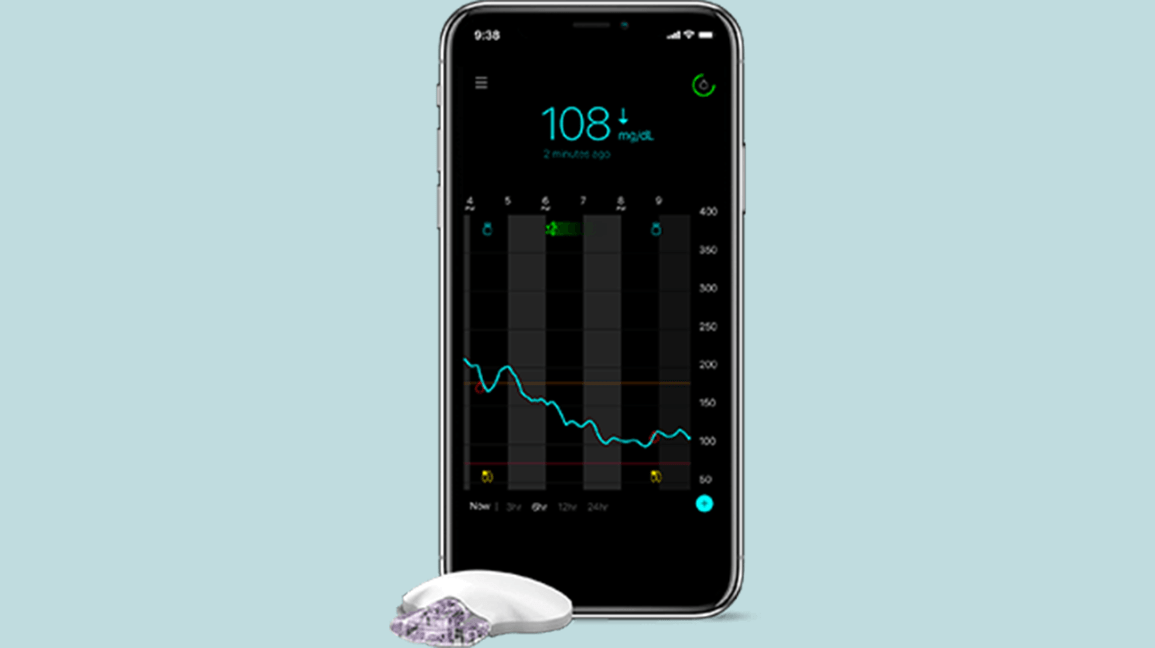
Im Gegensatz zum 670G-System, das keine Datenfreigabe oder Fernüberwachung bietet, bietet dieses eigenständige CGM integriertes Bluetooth Low Energy für die direkte Datenfreigabe mit einem Smartphone. Es verwendet denselben Guardian 3-Sensor, der für die Verwendung mit dem 670G zugelassen ist, und vermeidet insbesondere die Notwendigkeit eines separaten dedizierten Empfängers zur Anzeige der Daten.
Es ist nicht kalibrierungsfrei, was sich von konkurrierenden CGM-Produkten (Dexcom G5 und G6 und FreeStyle Libre-Versionen) unterscheidet, bei denen vor jeder Behandlung oder Insulindosierung keine Bestätigung durch einen Fingerabdruck erforderlich ist. Außerdem ist es erst für die Anwendung ab 14 Jahren zugelassen, was bedeutet, dass Kinder dieses Produkt nur erhalten können, wenn ein Arzt bereit ist, es „off-label“ zu verschreiben.
Guardian Connect-App für Mobilgeräte
Zum Zeitpunkt ihrer Einführung war diese kostenlose App nur für iOS-Benutzer verfügbar. Aber im Mai 2020 Medtronic gab die FDA-Zulassung bekannt für seine Android-Version ab Sommer. Es gibt jetzt auch einige ziemlich coole Snooze- und Anpassungsfunktionsupdates für die Blutzuckerverfolgung und -verwaltung, über die Sie hier lesen können.
Sugar.IQ-Mobile-App
Hierbei handelt es sich um eine separate mobile Anwendung, auf die Benutzer von Guardian Connect CGM ebenfalls exklusiven Zugriff haben. Es ist das Original IBM Watson-App das Medtronic erwarb und bewarb, bevor es 2017 schließlich einer begrenzten Anzahl von Kunden über sein eigenständiges CGM zugänglich gemacht wurde.
Die App verwendet IBM Watson Analytics, um Muster in Diabetesdaten zu finden und liefert in Echtzeit umsetzbare, personalisierte Erkenntnisse, darunter ein Kreisdiagramm mit Time-in-Range-Daten (TIR) und eine „glykämische Unterstützung“ für Informationen zu Lebensmitteln . Medtronic präsentiert wissenschaftliche Daten Dies zeigt, dass Personen, die das Guardian Connect-System mit der Sugar.IQ-App nutzen, 4,1 % mehr TIR erlebten als bei alleiniger Nutzung von Guardian Connect, was etwa einer zusätzlichen Stunde pro Tag entspricht. Darüber hinaus steigerten diejenigen, die auch die optionale glykämische Assist-Funktion nutzten, um ihre Reaktion auf bestimmte Lebensmittel zu untersuchen, die TIR um weitere 4 % im Vergleich zu denen, die diese Funktion nicht nutzten.

Zukünftige Produkte in Entwicklung
Unter neuer Führung seit Oktober 2019 hat der Geschäftsbereich Medtronic Diabetes vor der großen Konferenz der American Diabetes Association (ADA) im Juni 2020 einige interessante Details über seine nächste Technologiepipeline bekannt gegeben:
Erweiterter Hybrid-Closed-Loop (780G)
Erstmals vorgestellt bei den ADA Scientific Sessions im Juni 2019Das 780G Advanced Hybrid Closed Loop (ACHL)-System der nächsten Generation des Unternehmens wird den grundlegenden Formfaktor seiner Insulinpumpen der Modellreihe 6 haben. Dies bedeutet ein „modernes“ vertikales Aussehen im Vergleich zu älteren Modellen mit einem horizontalen Design, das an Pager erinnert die 1980er Jahre.
Einige Hauptmerkmale des 780G, die wir gelernt haben:
- verwendet einen neuen Algorithmus, den das Unternehmen als präziser und zuverlässiger erachtet und der im Anschluss an die entwickelt wurde Partnerschaft mit DreaMed Diabetes mit Sitz in Israel 2015 angekündigt.
- Funktioniert mit dem Zeus CGM-Sensor der nächsten Generation, der am ersten Tag nur eine Kalibrierung durchführt und danach keinen Fingerstich mehr erfordert.
- gibt alle 5 Minuten einen automatischen Korrekturbolus ab, um Benutzern dabei zu helfen, den optimalen Bereich beizubehalten und verpasste Mahlzeiten automatisch auszugleichen.
- hat einen einstellbaren Blutzuckerzielwert zwischen 100 und 120 mg/dl (im Vergleich zum festen Zielwert des 670G von 120 mg/dl).
- bietet im Gegensatz zu anderen kommerziell erhältlichen geschlossenen Kreislaufsystemen unterschiedliche Insulindauern.
- bietet das integrierte Bluetooth, das für die Datenfreigabe und Fernüberwachung erforderlich ist, sowie Over-the-Air-Remote-Software-Updates, sodass Benutzer nicht jedes Mal, wenn neue Funktionen eingeführt werden, ein völlig neues Gerät kaufen müssen. (Derzeit bietet nur das Tandem t:slim X2 diese Remote-Update-Funktion).
- Medtronic plant, die Aufsichtsbehörden zu bitten, dieses neue System von Anfang an für Erwachsene UND Kinder ab 2 Jahren zu genehmigen.
Während der ADA Sci-Sitzungen im Juni 2020 veröffentlichte Medtronic wichtige zentrale Testdaten für dieses kommende 780G-System, das bessere TIR-Ergebnisse und beeindruckende Benutzerzufriedenheitsbewertungen für die Benutzerfreundlichkeit des Systems zeigt.
Dieses System hat jetzt Genehmigung der CE-Kennzeichnung im Auslandund das Unternehmen bereitet sich darauf vor, den 780G bald hier in den Vereinigten Staaten bei der FDA einzureichen.
770G über Bluetooth verbunden
Medtronic erhielt am 31. August 2020 die FDA-Zulassung für sein 770G, die BLE-fähige Komponente seines kommenden 770G-Geräts. Dies gilt als Lückenbüßer zwischen dem bestehenden 670G und dem kommenden 780G und fügt Bluetooth-Konnektivität für den Datenaustausch und die Fernüberwachung hinzu (etwas, das Konkurrenzgeräte wie Dexcom seit Jahren anbieten). Es ist insbesondere für Kinder unter 6 Jahren und ab 2 Jahren verfügbar.
Medtronic bringt zunächst das 770G als separates Gerät auf den Markt, bevor schließlich das vollständige 780G auf den Markt kommt. Das Unternehmen weist darauf hin, dass Kunden problemlos aus der Ferne auf den 780G und neuere Funktionen upgraden können, anstatt neue Hardware kaufen zu müssen (ähnlich wie es Tandem mit seiner Remote-Update-Funktion im t:slim X2 bietet).
Infusionsset für längere Tragedauer
Kürzlich Medtronic Daten präsentiert auf seinem 7-Tage-Infusionsset, das doppelt so lange getragen werden kann wie aktuelle Sets, maximal 3 Tage. Eine entscheidende Studie in den Vereinigten Staaten läuft derzeit und dieses neue Infusionsset ist in Europa bereits zugelassen.
In Pressemitteilungen hebt Medtronic einen „neuen und proprietären Ansatz“ hervor, der den Abbau von Insulin und den Verlust von Konservierungsstoffen angeht – zwei Dinge, die zu Verstopfungen (Insulin verstopft die Pumpenschläuche) und damit zu einem höheren Blutzucker führen können. Zusätzlich zur Aufrechterhaltung der Insulinstabilität für volle 7 Tage sorgt die neue Klebetechnologie dafür, dass es während der gesamten Tragezeit am Körper haftet.
Frühe klinische Daten zeigen, dass Menschen, die dieses neue Set verwenden, 5 bis 10 Durchstechflaschen Insulin pro Jahr einsparen könnten, die derzeit verschwendet werden, da das Set alle drei Tage gewechselt werden muss. Weniger häufige Veränderungen insgesamt würden es auch anderen Hautstellen ermöglichen, sich auszuruhen und zu heilen, betont Medtronic.
Wir erinnern jedoch daran, dass Infusionsgeräte als „Achillesferse“ der modernen Insulinpumpentechnologie bezeichnet werden, da sie typischerweise viele Schwächen aufweisen. Insbesondere Medtronic hat in diesem Bereich nicht die erfolgreichste Erfolgsbilanz. Erinnern Sie sich an die BD FlowSmart-Technologie, die unter dem allgemeinen Namen Medtronic Pro eingeführt wurde? Dies hielt nicht lange an, da Berichte über verbogene Kanülen dazu führten, dass Medtronic das erste Produkt vom Markt nahm. Das Unternehmen arbeitete mit BD zusammen, um die Probleme zu untersuchen, und plante, dieses Infusionsset neu auf den Markt zu bringen Letztendlich gab BD das Konzept auf vollständig.
Zukünftige CGM-Sensoren
Medtronic entwickelt außerdem seine CGM-Sensoren der nächsten Generation und geht damit von den ursprünglichen Enlite-Sensoren und der aktuellen Version des Guardian 3, die mit dem Minimed 670G und einem eigenständigen CGM geliefert wird, einen Schritt weiter. Das Unternehmen deutete schon seit Jahren in wissenschaftlichen Präsentationen auf zukünftige CGMs hin, wurde aber erst Mitte 2020 öffentlich thematisiert.
Derzeit sind die beiden neuen Modelle unter internen Projektnamen bekannt, die wahrscheinlich nicht die endgültigen Markennamen sein werden:
- Projekt Zeus-Sensor: hätte immer noch 7 Tage Halt und das gleiche Muscheldesign, aber es wäre ein „iCGM“-Klassifizierung (Von der FDA für die Integration mit anderen Geräten zugelassen) und würde eine Fingerkalibrierung nur am ersten Tag der Verwendung erfordern.
- Projektsynergie: ein All-in-One-Sensor/Sender, der komplett wegwerfbar ist und ein neues Aussehen hat. Mit einem flacheren quadratischen Format, das 50 % kleiner als das aktuelle Modell ist, ist kein Überband zum Halten erforderlich und der Einführvorgang ist in drei Schritten einfacher und dauert nur 10 Sekunden. Es ist nicht sicher, ob es eine längere Tragedauer von 7 Tagen hat. Dies wird wahrscheinlich in mindestens ein oder zwei Jahren (ca. 2022–23) stattfinden, da experimentelle Studien gerade erst beginnen.
Benutzerdefinierter geschlossener Regelkreis
Medtronic arbeitet bereits an dieser zukünftigen Version seines Closed-Loop-Systems, die eine noch personalisiertere Steuerung über die Smartphone-Schnittstelle ermöglichen würde – mit automatischer Einstellungsoptimierung, optionaler automatischer Kohlenhydratabdeckung und KI (künstliche Intelligenz), die eine Anpassung ermöglicht. zum Patientenverhalten. Alles mit einem TIR-Ziel von 85 Prozent. Ein Teil davon würde wahrscheinlich die Übernahme von zwei Start-ups durch Medtronic umfassen: Nutrino-Gesundheit et Schlüsselzur Überwachung von Essgewohnheiten und zur Wissenschaft der Nährwertdaten.
Die Frage ist immer, wann etwas bei der FDA eingereicht, geschweige denn tatsächlich genehmigt wird, aber angesichts der FDA-Durchbruchsbezeichnung Für dieses Versuchsgerät im Jahr 2019 gewährt, ist es vielleicht nicht mehr allzu weit entfernt.
Dosierungsanspruch (plus Medicare-Deckung)
Medtronic hat den Status „nicht ergänzend“ für seine CGM-Sensoren nur zögerlich angestrebt, wodurch die Notwendigkeit einer Fingerabdruckbestätigung entfällt und eine Medicare-Abdeckung möglich wäre. Während alle anderen Wettbewerber von CGM diese FDA-Zulassung erhalten haben, hat Medtronic sich bei der Erlangung sehr viel Zeit gelassen.
Dennoch teilte das Unternehmen DiabetesMine mit, dass es bereits seit mehreren Jahren darüber nachdenke und beabsichtige, es bald für seinen Guardian 3-Sensor und sein 780G-System weiterzuverfolgen. Bei Genehmigung durch die Aufsichtsbehörden könnten das eigenständige Guardian 3 CGM-System des Unternehmens sowie sensorgestützte Geräte Anspruch auf Medicare-Versicherung haben.
Tubeless-Patchpumpe?
Es war einmal das Ziel von Medtronic Diabetes, eine Patch-Pumpe zu entwickeln, die nicht über die herkömmlichen Schläuche verfügte, über die die Geräte verfügten. Branchenbeobachter erinnern sich an den Plan des Unternehmens im Jahr 2008 – nur wenige Jahre nach der Markteinführung des schlauchlosen Omnipod –, eine eigene Einweg-Patchpumpe zu entwickeln.
Medtronic Diabetes hat diese Idee schon vor Jahren fast aufgegeben, aber hin und wieder wird sie erwähnt und weckt neues Interesse. Bis Mitte 2020 ist der Omnipod immer noch der einzige seiner Art, obwohl viele Möchtegern-Patchpumps gekommen und gegangen sind und immer noch über zukünftige Produkte sprechen.
Interoperabilitätspfad
Als Teil all dieser Zukunftstechnologien beschleunigt Medtronic die entscheidenden Tests, die zur Erlangung der begehrten „iCGM“-Interoperabilitätsklassifizierung erforderlich sind. Seit Mitte 2020 verfügt das Dexcom G6 über diese Bezeichnung, um mit der Closed-Loop-Technologie zu arbeiten, während das FreeStyle Libre 2 über eine eingeschränkte Version des iCGM-Status verfügt, was bedeutet, dass es derzeit nicht mit Geräten zur automatisierten Insulinverabreichung verwendet werden kann.
Im Juni 2019, Medtronic und Tidepool gaben bekannt Es würde in einem zukünftigen interoperablen geschlossenen Kreislauf betrieben werden – getrennt von den oben erwähnten 780G/AHCL- und benutzerdefinierten geschlossenen Kreislaufsystemen. Es ist unklar, wie weit es entfernt sein könnte und welche Funktionen es bieten könnte.
Verlassene Technologie
Wir haben endlich das Ende einer Ära gesehen, wenn es um die ursprünglichen Insulinpumpenmodelle von Medtronic geht, die im Jahr 2018 wie bunte Pager aussahen. Diese sind immer noch weit verbreitet, wurden aber jetzt offiziell eingestellt und sind nicht mehr im Handel erhältlich. Mit der Zeit wird es immer schwieriger, Vorräte zu finden.
Auf ihrem Höhepunkt war die Minimed 530 monumental, weil sie das tat, was keine andere Insulinpumpe zuvor getan hatte: Sie unterbrach automatisch die Insulinabgabe, wenn Sie einen bestimmten niedrigen Glukoseschwellenwert überschritten. Medtronic erhielt im September 2013 die FDA-Zulassung für diese Low-Glucose-Suspension (LGS) oder Threshold-Suspension-Funktion und blieb bis Oktober 2018 verfügbar, als Medtronic sie und die früheren „Serie 5“-Pumpen zugunsten neuerer Geräte der Serie 6 einstellte.
Ironischerweise verwenden viele Mitglieder der DIY-Diabetes-Innovationsgemeinschaft #WeAreNotWaiting immer noch diese älteren Modelle von Insulinpumpen, weil sie immer noch recht zuverlässig sind und – halten Sie Ihre Ohren, FDA und Diabetesberater sind bei minderwertigen Produkten vorsichtig. verwenden – kann gehackt werden.
Trotz einer Warnung der FDA und Bedenken der Mainstream-Medien im Jahr 2019, dass diese hausgemachten Systeme aufgrund ihrer veralteten Technologie nicht cybersicher seien, bleiben sie im Umlauf.
Zugang zu Diabetes Matters
Zugang und Erschwinglichkeit sind entscheidende Themen, die für zu viele Menschen in der Diabetikergemeinschaft ein Hindernis für den Zugang zu Technologie darstellen.
Der Versicherungsschutz spielt dabei eine große Rolle, aber leider war Medtronic in den letzten Jahren in dieser Hinsicht ein umstrittenes Unternehmen.
Im Rahmen seines Schritts hin zu einer „wertbasierten“ oder „ergebnisorientierten“ Pflege unterzeichnete Medtronic 2016 eine Vereinbarung mit dem Krankenversicherungsgiganten United Health Care (UHC), die die Pumpen von Medtronic zur „bevorzugten Marke“ für seine Produkte machte. Planinhaber. Im Jahr 2019 folgte ein ähnlicher Deal für die neueste für Kinder zugelassene Medtronic-Technologie.
Diese Einschränkung der Wahlmöglichkeiten hat, gelinde gesagt, viele Mitglieder der D-Community verärgert. Während UHC und Medtronic beide betonen, dass in manchen Fällen Ausnahmen gemacht werden können, erbittert sich der Kampf gegen diese Form der nichtmedizinischen Veränderung, die aus kommerziellen Gründen Vorrang vor den Präferenzen von Ärzten und Patienten hat. Glücklicherweise, Die CSU begann, eine Wahl anzubieten am 1. Juli 2020, als das Produktportfolio der Marke um die Tandem-Diabetes-Technologie sowie Medtronic-Produkte erweitert wurde.
Letztendlich kommt es auf die einfache Realität an #DiabetesAccessMatters. Keine Form von Innovation hat irgendeine Wirkung, wenn die Menschen sie nicht in die Hände bekommen.
Auch wenn Medtronic zweifellos Anerkennung dafür verdient, was es bei der Bereitstellung neuer Technologien für die Gemeinschaft erreicht hat, bitten wir sie, auch dabei zu helfen, die Wahlmöglichkeiten von Patienten und Ärzten zu fördern.
MEHR LESEN MEHR LESEN MEHR LESEN MEHR LESEN MEHR LESEN MEHR LESEN MEHR LESEN MEHR LESEN

